Curso de termodinâmica/Gases reais
|
| ||||
| Gases perfeitos | Gases reais | V der Waals | Est. corresp. | Outras |
Introdução
[editar | editar código-fonte]Experimentalmente, à baixa pressão, observe-se que muitos gases obedecem à equação de estado dos gases perfeitos. Porém há exceções. Por exemplo, o produto PV , em vez de ser constante numa certa temperatura, aumenta ou diminui quando P aumenta de zero para algumas atm.

Neste caso , o gás obedece mais a uma lei do tipo :
Onde B, que chamamos o segundo coeficiente do virial é negativo para as moléculas de grande tamanho CO2 ou O2 mas positivo para as moléculas de tamanho pequeno (Ne).

À maior pressão ainda , a variação de PV em relação de P não é linear .
A equação de estado que reproduz os dados experimentais é chamada equação de estado do virial.
onde B, C, D, ... são os coeficientes do virial do gás estudado.

Uma outra maneira de expressar os desvios em relação ao gás perfeito utiliza o parâmetro Z, fator de compressibilidade :
que é igual a 1 para um gás perfeito.
As observações experimentais indicam que Z = 1 unicamente quando P tende para zero. Em geral , Z é diferente de 1 para os gases reais . Pode se notar que grandes desvios são observados a baixa temperatura . A alta temperatura , ao contrario , o metano se comporta como um gás perfeito numa grande faixa de pressão.
Por exemplo , a T =200oC
Estes resultados mostram que :
Qualquer gás se comporta como um gás perfeito a
- pressão infinitamente baixa qualquer que seja a temperatura , ou a
- baixa pressão e alta temperatura.
Origem molecular dos desvios à lei dos gases perfeitos
[editar | editar código-fonte]À pressão elevada , qualquer que seja a temperatura , o desvio é positivo (Z> 1). Nestas pressões , o volume ocupado pelas moléculas não é mais irrisório em relação ao volume do recipiente . O volume das moléculas não é levado em conta na lei dos gases perfeitos. O volume disponível , em fato , é menor que V. Usar o volume do recipiente como valor de V, leva a valores exagerados de PV e a valores de Z maiores que 1. A temperatura e pressão baixas , o desvio , em geral , é negativo. A razão é que as moléculas de gás interagem . Por causa da polarizabilidade (ou do momento dipolar ), as moléculas se atraiam mutuamente, a pressão que elas sofrem é maior que aquela exercida nas paredes. PV é então menor que previsto e Z é menor que 1.
As atrações entre moléculas de gás conduzem o gás a se liquefazer se a temperatura é suficientemente baixa e a pressão suficientemente elevada . A passagem no estado líquido manifesta-se nas curvas de variação da pressão em função do volume a temperatura constante , por exemplo no caso do CO2.

A uma temperatura de 40 ou 50 oC , não há valores de pressão com CO2 líquido.
De um outro lado, a 21,5oC, CO2 se liquefaz quando a pressão chega a 60 atm.
À 0°C, o estado líquido aparece para P>35 atm aprox.
A maior temperatura onde pode se formar CO2 líquido é a temperatura crítica TC, aqui 31.04oC.
A pressão onde se forma o estado líquido nesta temperatura é a pressão crítica PC.
A TC e PC , o volume molar é o volume crítico VC.
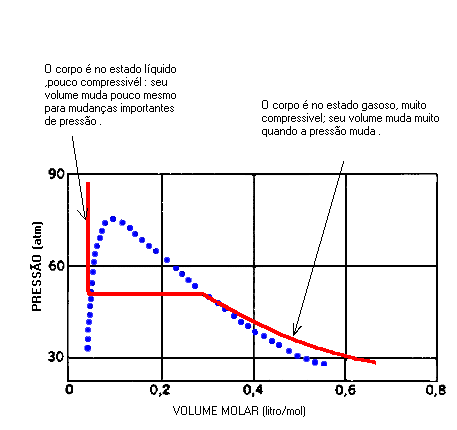
O traçado das isotermas que segue permite por em evidência diferenças entre o estado líquido e o estado gasoso .
A transição de um estado para um outro se acompanha de uma mudança importante do volume , à pressão e temperatura constantes
O estado onde se encontra um gás a temperatura um pouco maior a TC é peculiar por coisa da extrema sensibilidade do volume molar com a temperatura . É um fluido supercrítico no qual novas separações cromatográficas (caso do CO2) ou novas reações químicas (caso da água) podem acontecer .
Podemos representar as diversas regiões do gás , do líquido e do fluido supercrítico num diagrama a três dimensões P(V,T) cujos diagramas P(V) a seguir são as projeções num plano:
As variáveis críticas para alguns gases são apresentadas a seguir :
| Gás | (K) | Pc (bar) | Vc/n (cm3mol-1) | Zc |
|---|---|---|---|---|
| Nitrogênio N2 | 126,1 | 33,9 | 90,0 | 0,292 |
| Metano CH4 | 190,6 | 46,0 | 99;0 | 0,288 |
| Etileno C2H4 | 282,4 | 49,0 | 127,4 | 0,278 |
| Dióxido de Carbono CO2 | 304,2 | 74,0 | 96 |