Bioquímica/Estrutura e classificação dos aminoácidos
Estrutura e classificação dos aminoácidos
[editar | editar código-fonte]
Classificação
[editar | editar código-fonte]Os aminoácidos podem ser classificados nutricionalmente, quanto à sua cadeia lateral e quanto ao seu destino.
Aminoácidos essenciais e não essenciais
[editar | editar código-fonte]Um aminoácido essencial é aquele que o organismo (considerado normalmente, o humano) não é capaz de sintetizar mas é requerido para o seu funcionamento.
O organismo humano é incapaz de sintetizar cerca de metade dos vinte aminoácidos comuns. Tem então de os obter através da dieta, pela ingestão de alimentos ricos em proteínas.
Os aminoácidos não essenciais são também necessários para o funcionamento do organismo, mas podem ser sintetizados in vivo a partir de determinados metabolitos.
Existem aminoácidos que são essenciais apenas em determinadas situações patológicas ou em organismos jovens e em desenvolvimento. A estes convencionou-se a designação "condicionalmente essenciais". Estes aminoácidos são normalmente fonte de divisão entre os cientistas, havendo os que consideram estes como essenciais e os que não os consideram essenciais.
| Não essenciais | Condicionalmente essenciais | Essenciais |
|---|---|---|
| Alanina | Arginina | Histidina |
| Asparagina | Glutamina | Isoleucina |
| Aspartato | Glicina | Leucina |
| Glutamato | Prolina | Lisina |
| Serina | Tirosina | Metionina |
| Cisteína | Fenilalanina | |
| Treonina | ||
| Triptofano | ||
| Valina |
Os aminoácidos não essenciais possuem, em geral, vias de síntese relativamente simples. Por exemplo, o metabolito α-cetoglutarato (intermediário do ciclo dos ácidos tricarboxílicos) é precursor do glutamato, que por sua vez pode dar origem à glutamina, à prolina e à arginina.
Quanto à cadeia lateral
[editar | editar código-fonte]A classificação quanto à cadeia lateral (a negrito) pode ser feita em: Aminoácidos Apolares e Polares. Com uma subdivisão dos polares em Aa polares neutros; Aa polares ácidos e Aa polares básicos.
- Aminoácidos apolares
Apresentam grupos químicos de hidrocarbonetos apolares ou hidrocarbonetos modificados, exceto a glicina (que possui um átomo de hidrogénio como cadeia lateral). São hidrófobos.
- Glicina: H-CH(NH2) -COOH
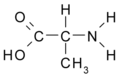
- Alanina: CH3-CH(NH2) -COOH
- Leucina: CH3(CH3)-CH2-CH(NH2)-COOH
- Valina: CH3-CH(CH3)-CH(NH2)-COOH
- Isoleucina: CH3-CH2-CH (CH3)-CH(NH2)-COOH
- Prolina:-CH2-CH2-CH2- ligando o grupo amino ao carbono alfa
- Fenilalanina: C6H5-CH2-CH(NH2)-COOH
- Triptofano: R aromático-CH(NH2)-COOH
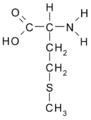
- Metionina: CH3-S-CH2-CH2-CH(NH2)-COOH
- Aminoácidos Polares neutros
Apresentam grupos químicos que tendem a formar ligações de hidrogénio.
- Serina: OH-CH2-CH(NH2)-COOH
- Treonina: OH-CH (CH3)-CH(NH2)-COOH
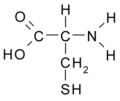
- Cisteina: SH-CH2-CH(NH2)-COOH
- Tirosina: OH-C6H4-CH2-CH(NH2)-COOH
- Asparagina: NH2-CO-CH2-CH(NH2)-COOH
- Glutamina: NH2-CO-CH2-CH2-CH(NH2)-COOH
- Aminoácidos Polares ácidos
Apresentam grupos carboxilato.São hidrófilos.
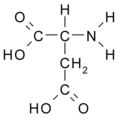
- Ácido aspártico: HCOO-CH2-CH(NH2)-COOH
- Ácido glutâmico: HCOO-CH2-CH2-CH(NH2)-COOH
- Aminoácidos Polares básicos
Apresentam grupos amino. São hidrófilos.
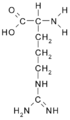
- Arginina: HN=C(NH2)-NH-CH2-CH2-CH2-CH(NH2)-COOH
- Lisina: NH2-CH2-CH2-CH2-CH2-CH(NH2)-COOH
- Histidina: H-(C3H2N2)-CH2-CH(NH2)-COOH
Quanto ao destino
[editar | editar código-fonte]Essa classificação é dada em relação ao destino tomado pelo aminoácido quando o grupo amina é excretado do corpo na forma de ureia (mamíferos), amônia (peixes) e ácido úrico (aves e répteis).
- Destino cetogênico
Quando o álcool restante da quebra dos aminoácidos vai para qualquer fase do ciclo dos ácidos tricarboxílicos sob a forma de acetil-coenzima A ou outra substância.
- Destino glicogênico
Quando o álcool restante da quebra dos aminoácidos vai para a glicólise.
Fórmula estrutural
[editar | editar código-fonte]-
Alanina (Ala/A)
-
Arginina (Arg/R)
-
Asparagina (Asn/N)
-
Ácido aspártico (Asp/D)
-
Cisteina (Cys/C)
-
Ácido glutâmico (Glu/E)
-
Glutamina (Gln/Q)
-
Glicina (Gly/G)
-
Histidina (His/H)
-
Isoleucina (Ile/I)
-
Leucina (Leu/L)
-
Lisina (Lys/K)
-
Metionina (Met/M)
-
Fenilalanina (Phe/F)
-
Prolina (Pro/P)
-
Serina (Ser/S)
-
Treonina (Thr/T)
-
Triptofano (Trp/W)
-
Tirosina (Tyr/Y)
-
Valina (Val/V)
Estrutura tridimensional
[editar | editar código-fonte]Aminoácidos apolares
[editar | editar código-fonte]-
Glicina (Gly/G)
-
Alanina (Ala/A)
-
Leucina (Leu/L)
-
Isoleucina (Ile/I)
-
Valina (Val/V)
-
Metionina (Met/M)
-
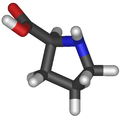
Prolina (Pro/P)
-
Fenilalanina (Phe/Fen)
-
Triptofano (Trp/W)
Aminoácidos polares neutros
[editar | editar código-fonte]-
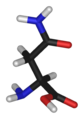
Asparagina (Asn/N)
-
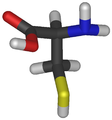
Cisteína (Cys/C)
-
Glutamina (Gln/Q)
-
Serina (Ser/S)
-
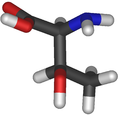
Treonina (Thr/T)
-
Tirosina (Tyr/y)
Aminoácidos polares ácidos
[editar | editar código-fonte]-
Ácido aspártico (Asp/D)
-
Ácido glutâmico (Glu/E)
Aminoácidos polares básicos
[editar | editar código-fonte]-
Lihsina (Lys/K)