Bioquímica/Aminoácidos
| Este módulo precisa ser revisado por alguém que conheça o assunto (discuta). |
Aminoácidos
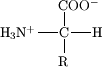
Os aminoácidos são moléculas que contêm simultaneamente grupos funcionais amina e ácido carboxílico. Em Bioquímica, este termo é usado como termo curto e geral para referir os aminoácidos alfa, ou seja, aqueles em que as funções amino e carboxilato estão ligadas a um carbono alifático, denominado carbono-alfa (carbono-α). Pelo menos um átomo de hidrogênio está ligado a este carbono. A esfera de coordenação do carbono-α é completada com a presença de uma cadeia lateral, diferente para diferentes aminoácidos. Os aminoácidos α (cerca de vinte) são constituintes de todas as proteínas e peptídeos.
Em soluções aquosas de pH neutro, os aminoácidos podem existir em duas formas. Uma pequena fração encontrar-se-á numa forma eletricamente neutra, ou seja, com o grupo amina desprotonado (-NH2) e o grupo carboxilo protonado (-COOH). A maioria estará, no entanto, numa forma ionizada, em que o grupo amina se encontra protonado (-NH3+) e o ácido carboxílico desprotonado a carboxilato (-COO-), denominando-se esta forma de zwitteriónica (do alemão zwitter, que significa "híbrido"). Um zwitterião é uma molécula globalmente neutra em termos de carga elétrica mas possuindo cargas locais devido à presença de grupos ionizados.
Os aminoácidos podem ligar-se entre si com uma ligação amida, que em Bioquímica é especificamente designada, neste caso, de ligação peptídica. A ligação ocorre entre o átomo de carbono do grupo carboxilato e o nitrogênio do grupo amina; no processo, é libertada uma molécula de água, seno a ligação final entre o carbono de um grupo carbonilo e o nitrogênio de uma amina secundária. Como consequência, uma cadeia peptídica, ou seja, formada por diversos aminoácidos ligados desta forma, terá um grupo amina numa extremidade (denominada N-terminal) e um grupo carboxilato na extremidade oposta (denominada C-terminal).
A ligação peptídica tem uma geometria planar porque existe ressonância entre o grupo carbonilo e o nitrogênio da amina, fazendo com que a ligação C-N tenha um caráter parcial de ligação dupla (é possível desenhar uma estrutura de ressonância entre o átomo de carbono e o de nitrogênio, tendo uma carga negativa formal sobre o oxigênio e uma positiva sobre o nitrogênio). Esta característica impede que haja rotação em torno da ligação C-N, que se mantém numa conformação trans. Seis átomos encontram-se então no mesmo plano geométrico: o carbono-α de um aminoácido, os átomos do grupo carbonilo da ligação peptídica, os átomos da amina secundária dessa mesma ligação e o carbono-α do segundo aminoácido.
Simbologia e nomenclatura
Na nomenclatura dos aminoácidos, a numeração dos carbonos da cadeia principal é iniciada a partir do carbono do grupo carboxilato.
| Nome vulgar | Símbolo (3 letras) | Símbolo (1 letra) | Nome sistemático |
|---|---|---|---|
| Glicina ou Glicocola | Gly | G | Ácido 2-aminoacético ou ácido 2-amino-etanóico |
| Alanina | Ala | A | Ácido 2-aminopropiónico ou ácido 2-amino-propanóico |
| Leucina | Leu | L | Ácido 2-aminoisocapróico ou ácido 2-amino-4-metil-pentanóico |
| Valina | Val | V | Ácido 2-aminovalérico ou ácido 2-amino-3-metil-butanóico |
| Isoleucina | Ile | I | Ácido 2-amino-3-metil-n-valérico ou ácido 2-amino-3-metil-pentanóico |
| Prolina | Pro | P | Ácido pirrolidino-2-carboxílico |
| Fenilalanina | Phe | F | Ácido 2-amino-3-fenil-propiônico ou ácido 2-amino-3-fenil-propanóico |
| Serina | Ser | S | Ácido 2-amino-3-hidroxi-propiónico ou ácido 2-amino-3-hidroxi-propanóico |
| Treonina | Thr | T | Ácido 2-amino-3-hidroxi-n-butírico |
| Cisteína | Cys | C | Ácido 2-bis-(2-amino-propiónico)-3-dissulfeto ou ácido 3-tiol-2-amino-propanóico |
| Tirosina | Tyr | Y | Ácido 2-amino-3-(p-hidroxifenil)propiónico ou paraidroxifenilalanina |
| Asparagina | Asn | N | Ácido 2-aminossuccionâmico |
| Glutamina | Gln | Q | Ácido 2-aminoglutarâmico |
| Aspartato ou ácido aspártico | Asp | D | Ácido 2-aminossuccínico ou ácido 2-amino-butanodióico |
| Glutamato ou ácido glutâmico | Glu | E | Ácido 2-aminoglutárico |
| Arginina | Arg | R | Ácido 2-amino-4-guanidina-n-valérico |
| Lisina | Lys | K | Ácido 2,6-diaminocapróico ou ácido 2,6-diaminoexanóico |
| Histidina | His | H | Ácido 2-amino-3-imidazolpropiónico |
| Triptofano | Trp | W | Ácido 2-amino-3-indolpropiónico |
| Metionina | Met | M | Ácido 2-amino-3-metiltio-n-butírico |
Ponto isoelétrico
O ponto isoelétrico (pI) de uma molécula é o pH ao qual essa molécula é eletricamente neutra. Este conceito é aplicado particularmente a aminoácidos e proteínas. O ponto isoelétrico não é o pH em que todas os grupos básicos estão desprotonados e os ácidos protonados, mas antes o pH em que o número de cargas positivas e negativas da molécula se cancelam a zero.
O pI corresponde à média dos valores de pKa da molécula:
- pI=(pK1+pK2+...+pKn)/n
No caso de aminoácidos isolados com cadeias laterais ionizáveis, o pI do aminoácido será a média dos pKa dos grupos amino e carboxilato ligados ao carbono-α e ainda do pKa da cadeia lateral. As proteínas têm normalmente cadeiasionizáveis, e a diferente proporção de diferentes aminoácidos em cada tipo de proteína confere-lhes diferentes valores de pI.
O cálculo teórico de pI torna-se mais difícil quanto maior for a proteína, já que o pI das cadeias laterais de aminoácidos podem variar ligeiramente dentro do ambiente proteico. É no entanto possível fazer a determinação experimental do pI através de eletroforese em gel de poliacrilamida. A proteína cujo pI se pretende determinar é aplicada num gel ao longo do qual existe variação de pH; ao aplicar-se uma diferença de potencial entre as duas extremidades do gel, a proteína migra através deste até encontrar uma zona de pH igual à do seu pI. Neste ponto, a sua migração para, pois a carga da proteína é neutra a esse pH e não responderá mais à aplicação de um potencial elétrico. Esse valor de pH será então o pI da proteína.
Isomeria
Todos os aminoácidos obtidos pela hidrólise de proteínas em condições suficientemente suaves apresentam atividade óptica, à exceção da glicina. Como os aminoácidos apresentam quatro grupos diferentes ligados ao carbono central, os aminoácidos apresentam quiralidade, sendo o carbono-α um centro quiral.
O centro quiral permite a existência de estereoisômeros, devido aos diferentes arranjos espaciais possíveis, apresentando os aminoácidos uma atividade óptica. Mais especificamente, existem diferentes enantiômeros, ou seja, formas de aminoácidos que são a imagem do espelho uma de outra. Os enantiómeros de aminoácidos são usualmente classificados como D ou L, sendo essa classificação referente à semelhança com a estrutura do D-gliceraldeído e do L-gliceraldeído, respectivamente. Somente os L-aminoácidos são constituintes das proteínas.
Síntese
Todos os aminoácidos são derivados de intermediários da glicólise, do ciclo dos ácidos tricarboxílicos ou das via das pentoses-fosfato. O nitrogênio entra nessas vias através do glutamato. Há uma grande variação no nível de complexidade das vias, sendo que alguns aminoácidos estão a apenas alguns passos enzimáticos dos seus precursores e em outros as vias são complexas, como no caso dos aminoácidos aromáticos.
As vias biossintéticas de aminoácidos são agrupadas de acordo com a família dos precursores de um deles. As principais famílias são:
- A do α-cetoglutarato, que origina o glutamato, a glutamina, a prolina e a arginina.
- A do 3-fosfoglicerato, de onde são derivados a serina, a glicina e a cisteína.
- A do oxaloacetato, que dá origem ao aspartato, que vai originar a asparagina, a metionina, a treonina e a lisina.
- A do piruvato, que dá origem a alanina, a valina, a leucina e a isoleucina.
