Engenharia genética/Amplificação por PCR do gene GFP de Aequorea victoria: diferenças entre revisões
| [edição não verificada] | [edição não verificada] |
Conteúdo apagado Conteúdo adicionado
Sem resumo de edição |
Sem resumo de edição |
||
| Linha 6: | Linha 6: | ||
== Preparação das soluções para PCR == |
== Preparação das soluções para PCR == |
||
[[Imagem:PCR tubes.png|thumb|right| |
[[Imagem:PCR tubes.png|thumb|right|150px|Conjunto de oito tubos de PCR, cada um contendo 100μL.]] |
||
* Fazer uma diluição de 50X, em 2 tubos ''eppendorf'' marcados |
* Fazer uma diluição de 50X, em 2 tubos ''eppendorf'' marcados, fazendo 2 diluições sucessivas de 10X a partir de 100 μL de Taq e 900 μL do tampão de diluição 1X e depois 5X (200 μL → 800 μL); |
||
* Fazer 3 diluições sucessivas de 2X em 3 tubos ''eppendorf'' marcados |
* Fazer 3 diluições sucessivas de 2X em 3 tubos ''eppendorf'' marcados, a partir de 500 μL da diluição de 1000X e 500 μL de tampão de diluição 1X; |
||
* Colocar 20 μL das diluições em diferentes tubos de PCR: 10x, 50x, 100x, 200x e 400x (5 tubos); |
* Colocar 20 μL das diluições em diferentes tubos de PCR: 10x, 50x, 100x, 200x e 400x (5 tubos); |
||
| Linha 18: | Linha 18: | ||
* Colocar os tubos em gelo; |
* Colocar os tubos em gelo; |
||
[[Imagem:Serial Dilution (to PCR).jpg|thumb|centre| |
[[Imagem:Serial Dilution (to PCR).jpg|thumb|centre|900px|Preparação de soluções de DNA polimerase com diferentes concentrações, através da técnica de diluições seriais, para amplificação em PCR. Os factores de diluição correspondentes a cada solução estão representados nos rótulos dos respectivos eppendorfs. Pipetaram-se 100μL da solução inicial (1x) para o 1º eppendorf e adicionaram-se 900μL de Tampão de Diluição. Agitar a solução. Desta solução (10x) pipetaram-se 200μL para o 2º eppendorf e adicionaram-se 800μL de Tampão de Diluição. E assim sucessivamente, como descrito na figura, sempre de modo a perfazer 1mL de volume final no eppendorf. De todos esses eppendorfs retiraram-se 20μL aos quais se adicionou igual volume de Mastermix. Agitar as soluções. Inserir no termociclador, para realizar o PCR.]] |
||
Revisão das 19h40min de 27 de fevereiro de 2008
acima: ÍNDICE
Preparação das soluções para PCR

- Fazer uma diluição de 50X, em 2 tubos eppendorf marcados, fazendo 2 diluições sucessivas de 10X a partir de 100 μL de Taq e 900 μL do tampão de diluição 1X e depois 5X (200 μL → 800 μL);
- Fazer 3 diluições sucessivas de 2X em 3 tubos eppendorf marcados, a partir de 500 μL da diluição de 1000X e 500 μL de tampão de diluição 1X;
- Colocar 20 μL das diluições em diferentes tubos de PCR: 10x, 50x, 100x, 200x e 400x (5 tubos);
- Adicionar 20 μL de PCR MasterMix a cada tubo de PCR;
- Colocar os tubos em gelo;

- Depois de agitadas no vortex, as misturas são sujeitas a PCR de acordo com as condições especificadas na
tabela abaixo.
Condições do PCR
| Temperatura | Duração | Fase |
| 94 ºC | 120 seg | Desnaturação inicial |
| 94 ºC | 20 seg | Desnaturação |
| 40 ºC | 20 seg | Emparelhamento |
| 72 ºC | Taq = 20 seg e Pfu= 1 min 45 seg | Elongamento |
| 72 ºC | 120 seg | Elongamento final |
Esta sequência é repetida 30 vezes.
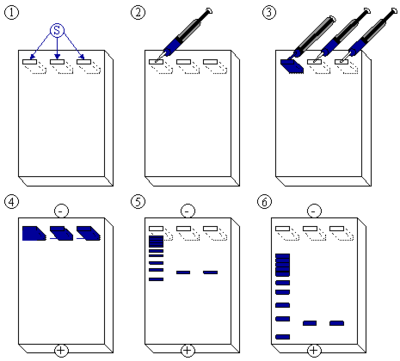
Análise Electroforética dos produtos de PCR
- Misturar 5 μL de produto de PCR com 5 μL de tampão de aplicação;
- Aplicar as amostras num gel de agarose 0,8%;
- O instrutor efectua a electroforese com as amostras correspondentes aos produtos de PCR de referência;
- Correr o gel, durante 20 minutos, a 220 volts;
- Fotografar o gel.

Actividades propostas
- Comparar o rendimento do PCR obtido com o da Taq polimerase comercial.
- Calcular o número de unidades na preparação.
